無機物質について、問1~3に答えよ。

解答 ④
解説
赤リンは暗赤色で無毒の粉末で黄リンを空気を絶って約250℃に長時間放置すると得られる。また、発火剤としてマッチの側薬に利用されており、赤リンに点火すると激しく白煙をあげて燃焼し十酸化四リンP4O10を生成する。この生成した十酸化四リンP4O10は脱水作用や吸湿性が強いので脱水剤や乾燥剤として用いられている。また、十酸化四リンP4O10に水を加えて煮沸するとリン酸H3PO4が得られ、その水溶液は中程度の酸性を示す。一方、黄リンは淡黄色のろう状の固体で極めて毒性が強く、空気中で酸化されて自然発火する。そのため水中に保存される。したがって、答えは④である。
これだけは押さえよう!!
<リンとその化合物の性質>
・リンは天然にはリン酸塩としてリン鉱石に含まれ、動物の体の骨や歯の成分にもなっている
・リンの同素体(同じ元素からなる単体)には5種類ありそのうち代表的なものが赤リンと黄リンである
【赤リンの性質】
・暗赤色の粉末
・無毒で自然発火しない
・マッチの側薬に利用
【黄リンの性質】
・淡黄色でろう状の固体
・有毒で自然発火する(石油中に保存)
・ねずみ取りの毒薬に利用
・十酸化四リンP4O10の性質
・白色の粉末で脱水作用や吸湿性が強いので脱水剤や乾燥剤として利用
・水を加えて煮沸するとリン酸H3PO4が得られ、その水溶液は酸性を示す
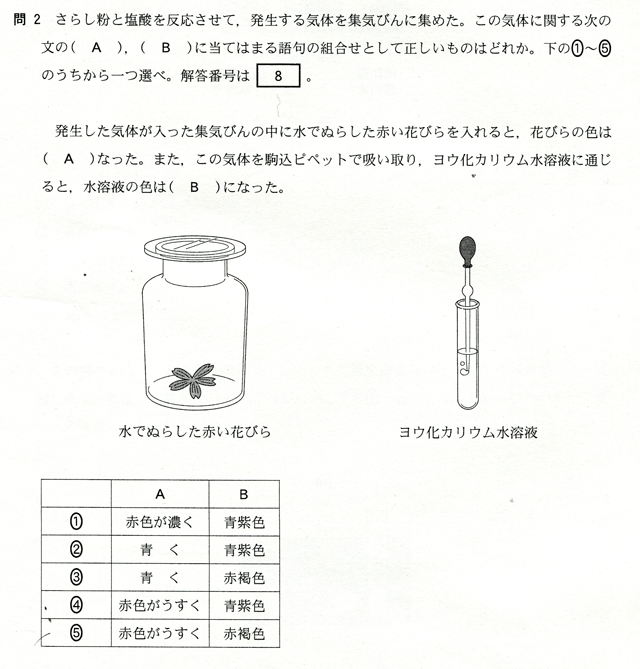
解答 ⑤
解説
さらし粉CaCl(ClO)に塩酸HClを作用させると以下の反応が起こり塩素Cl2が発生する。
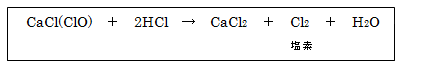
そして、この発生した塩素Cl2の中に花びらを入れると塩素Cl2は酸化力が強く漂白作用があるので花びらの赤色が薄くなる。一方、この発生した塩素Cl2をヨウ化カリウム水溶液の中に通じると以下の反応が起こりヨウ素が生成し、水溶液は赤褐色に変色する。
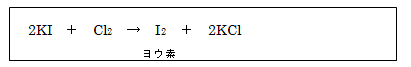
したがって、答えは⑤である。
これだけは押さえよう!!
・ハロゲンは17族の元素群で価電子を7個持ち、1価の陰イオンになりやすい
・ハロゲンはいずれも二原子分子からなり有毒である
表中の........を引いた部分は特に重要である
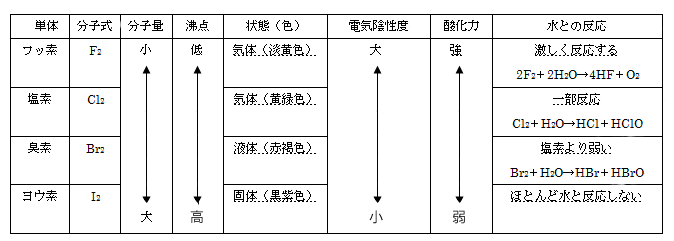
<塩素の製法>
・さらし粉CaCl(ClO)に塩酸HClを作用させる

・酸化マンガン(Ⅳ)に濃塩酸HClを加え加熱する
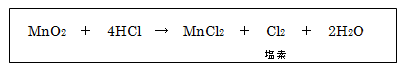
解答 ⑤
解説
塩酸や希硫酸には溶解せず硝酸や熱濃硫酸に溶解する金属は銅Cu、水銀Hg、銀Agのいずれかである。そのうち、空気中の水分H2Oと二酸化炭素CO2が作用して緑青と呼ばれる緑色のさびを生じるのは銅Cuであり、銅Cuと亜鉛Znの合金を黄銅と呼び、金管楽器や五円硬貨などに用いられている。したがって答えは⑤である。
これだけは押さえよう!!
<金属のイオン化傾向とその反応性>
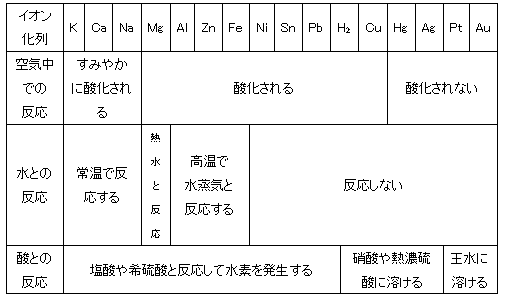
※なお、Pbは塩酸や希硫酸にほとんど溶解せず沈殿物をつくる。
また、Al、Fe、Ni は濃硝酸には溶けない。
・黄銅…銅Cuと亜鉛Znからなる合金